EN_Version
La ricerca farmaceutica ha beneficiato nel nuovo secolo di alcune scoperte epocali, che hanno reso più semplice capire cause ed effetti di malattie gravi – RNA interference, CRISPR-Cas9; sviluppare biomolecole naturali o modificate come soluzioni terapeutiche – anticorpi, vaccini, nucleotidi antisenso; e guidare principi attivi verso il proprio obiettivo molecolare, riducendo la tossicità per l’organismo – terapie mirate, nanopresentazione, drug delivery.
Nel nostro gruppo di UniMI (Università degli Studi di Milano), pur prendendo atto di queste importanti novità, non dimentichamo un vecchio forziere, pieno di ricchezze ancora in gran parte da scoprire e da valorizzare:
le piccole molecole organiche, siano esse il risultato di un approccio razionale a un bersaglio molecolare – derivati di sintesi – o il risultato dell’evoluzione per dotare un organismo vivente di un vantaggio competitivo nel suo ambiente – prodotti naturali.
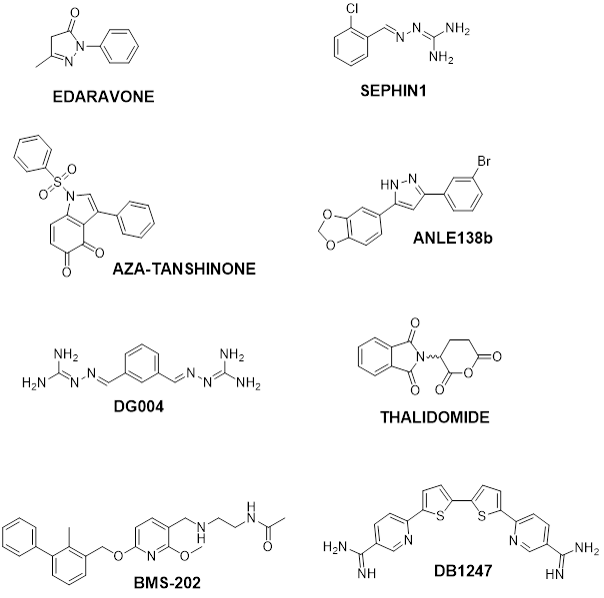
Il nostro lavoro di “taglio e cucito” su piccole molecole organiche è diretto verso le malattie neurodegenerative ed il cancro, cioè gli stessi obiettivi del progetto NEVERMIND; il nostro scopo è, per ognuna delle molecole mostrate in Figura, diverso ma rilevante per scopi terapeutici; ognuna di esse potrebbe diventare in futuro un cargo da veicolare attraverso nanooggetti intelligenti NEVERMIND-like nel cervello di pazienti.
La chimica di sintesi può supportare l’identificazione di un nuovo bersaglio molecolare, o l’elucidazione di un meccanismo patologico, attraverso la sintesi di strumenti (chemical probes) capaci di interagire con un bersaglio sconosciuto, o di essere “visibili”-fluorescenti in un intorno cellulare, o addirittura in un organismo vivente; a questo scopo stiamo preparando probes derivati da molecole note ed attive in vivo, di cui non è noto il bersaglio molecolare.
Fra loro l’edaravone (farmaco approvato per il trattamento della SLA), sephin1 (in clinica per la sessa malattia) ed un nostro derivato sintetico dei tanshinoni naturali (aza-tanshinone, antitumorale attivo attraverso varie interazioni molecolari da chiarire).
Possiamo anche combinare due piccole molecole note, con meccanismi d’azione diversi, in un unico dual action compound: ad esempio, l’anti-aggregante anle138b, specifico per a-sinucleina, e la talidomide, ligando della proteina E3 ligasi Cereblon ad attivare la degradazione proteica via proteasoma, per ottenere la rapida eliminazione di fibrille ed oligomeri abbondanti nelle sinucleinopatie come il morbo di Parkinson.
Infine, con l’aiuto di modelli computazionali, cerchiamo di disegnare la “mano perfetta” (piccola molecola) che riempia perfettamente un”guanto” terapeuticamente rilevante (sito attivo del bersaglio molecolare).
Abbiamo sviluppato DG004, uno stabilizzatore del complesso retromerico a ripristinare lo smaltimento di aggregati tossici che ha ottima efficacia in modelli in vivo di SLA; e stiamo lavorando per sviluppare analoghi innovativi e brevettabili di BMS-202 (peptidomimetico in grado di riattivare il sistema immunitario contro il cancro attraverso la prevenzione dell’interazione fra PD-1 e PD-L1) e di DB1247 (ligando di strutture G-quadruplex ripetitive dell’RNA di c9orf72, potenzialmente utile per la cura di demenza frontotemporale e SLA).


 Il Prof. Seneci è PI dell’Unità dell’Università degli Studi di Milano, Partner del progetto NEVERMIND.
Il Prof. Seneci è PI dell’Unità dell’Università degli Studi di Milano, Partner del progetto NEVERMIND.

